卵巢癌领域研究进展(三)
作者:肿瘤瞭望 日期:2020/5/21 10:33:04 浏览量:35597
肿瘤瞭望版权所有,谢绝任何形式转载,侵犯版权者必予法律追究。
日前,拟于在加拿大多伦多举办的第51届美国妇科肿瘤学会(SGO)年会因新冠疫情影响,被迫取消线下会议。SGO官网公布会议摘要内容,本文就大会公布的卵巢癌相关摘要进行了整理,供读者学习。
1、【35 – Seminal Abstracts】Population adjusted indirect comparison of the SOLO1 and PAOLA-1/ENGOT-ov25 studies of olaparib with or without bevacizumab, bev alone and placebo in the maintenance treatment of women with newly diagnosed stage III/IV ovarian cancer with BRCA mutation
?
人群调整后间接对比SOLO1和PAOLA-1/ENGOT-ov25研究:奥拉帕利联合或不联合贝伐珠单抗VS贝伐珠单抗或安慰剂维持治疗新诊断的BRCA突变III/IV期卵巢癌患者。
目的:研究者的目的是评估奥拉帕利联合或不联合贝伐珠单抗、奥拉帕利 vs 贝伐珠单抗、贝伐珠单抗 vs 安慰剂在新诊断BRCA突变III/IV期卵巢癌患者维持治疗中的疗效。方法:根据研究调查者的意见,使用来自SOLO1(奥拉帕利 vs 安慰剂)的患者数据,与来自PAOLA-1(奥拉帕利+贝伐珠单抗 vs 安慰剂+贝伐珠单抗)BRCA突变亚组的患者数据合并,针对研究终点PFS进行了一项非锚定总体调整的间接比较(PAIC)。用治疗权重的反向概率将PAOLA-1的队列与SOLO1队列相匹配,使得关键的基线临床和人口学特征在不同人群中保持一致。所有分析均在拥有完整基线数据的患者中进行。采用加权Cox回归分析评估不同治疗方案的疗效,并辅以加权Kaplan-Meier进行补充分析。结果:从SOLO1获得完整基线数据患者380名,其中奥拉帕利组254名,安慰剂组126名。PAOLA-1中具有完整基线数据的携带BRCA突变的患者有222名,其中奥拉帕利+贝伐珠单抗组151名,安慰剂+贝伐珠单抗组71名。在配对之前,2年无进展比率为:奥拉帕利+贝伐珠单抗76%,奥拉帕利单药73%,安慰剂+贝伐珠单抗44%,安慰剂组36%。分配给PAOLA-1队列的权重范围为0.12到3.98(中位值0.88),有效样本量为166。匹配的PAOLA-1队列的基线数据与SOLO1相当,85%的FIGO III期患者,81%患者一线化疗后完全缓解,75%患者手术后无残留病灶。结论:PAIC的结果表明,在携带BRCA突变的新诊断卵巢癌患者中,奥拉帕利联合贝伐珠单抗与单独使用奥拉帕利进行一线维持治疗相比,在PFS方面有潜在的有意义的改善。贝伐珠单抗的临床益处表现出相加效应,并且在不同的方案中保持一致,例如当贝伐珠单抗与奥拉帕利联合 vs 奥拉帕利单药,贝伐珠单抗单药 vs 安慰剂时,会表现出相似的临床获益。尽管进行了匹配,但本分析的结果仍受到限制,因为它是一个非随机化的比较。
*目前奥拉帕利联合贝伐珠单抗治疗卵巢癌的适应症在中国尚未获批,目前奥拉帕利在中国获批的适应症为:携带胚系或体细胞BRCA 突变的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌初治成人患者在一线含铂化疗达到完全缓解或部分缓解后的维持治疗,铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。本材料所提供的相关信息在任何情况下均不应作为治疗或使用建议,亦不用于推广目的。
2、【5 - Scientific Plenary】A pilot study of nivolumab in combination with front-line neoadjuvant dose-dense paclitaxel and carboplatin chemotherapy in patients with high-grade serous ovarian cancer
纳武单抗联合一线新辅助剂量密集型紫杉醇+卡铂治疗高级别浆液性卵巢癌的初步研究
目的:在上皮性卵巢癌(EOC)患者中,肿瘤内T细胞计数增加与较好的预后相关,为纳武单抗等PD-1抑制剂的联合使用提供了理论依据。本研究探索了纳武单抗联合卡铂+紫杉醇周疗新辅助方案治疗EOC。首要终点是通过剂量限制性毒性(DLTs)来评价治疗安全性和耐受性。次要终点包括完全清除率(CGR)、化疗反应评分(CRS)、无进展生存期(PFS)、总生存期及一系列转化性参数。方法:研究选择FIGO III/IV期、适用于新辅助化疗和间歇性减瘤术(IDS)治疗的EOC患者。每周静脉注射紫杉醇(80mg/m2)联合每3周给予卡铂(AUC6)和纳武单抗(360mg)治疗。允许术前3-6个周期、总计6-8个周期的化疗。化疗结束后,可持续使用纳武单抗至1年。按CTCAE v4.0标准记录不良反应。行间歇性减瘤术时评估化疗反应评分(1-3分)(结果已发表)。还会对治疗前后的肿瘤标本进行多重免疫荧光检测。结果:共纳入21例患者,中位年龄64岁(38~77岁),白种人为主(81%),多数是高级别浆液型癌(90%)并处于IV期(67%)。一名患者在第一个周期治疗中发生3级输液反应后被替换出组。治疗耐受性良好:2例患者(9.5%)出现剂量限制性毒性(4级肺炎,4级肌炎),推迟了IDS。由纳武单抗引起的其他3-4级不良事件包括:皮疹(10%)、发热(5%)、疲乏(5%);19%的患者出现2级甲减;90%患者达到最佳CGR;35%患者的CRS评分为3分。中位PFS尚未达到;71.9%的患者在1年内无进展,中位随访时间14.3个月(6.3-19.8月)。所有病人都健在。治疗与肿瘤微环境向“炎症型”表型转化有关,CD8+T细胞百分比显著增加(P=0.0002)(图1)。
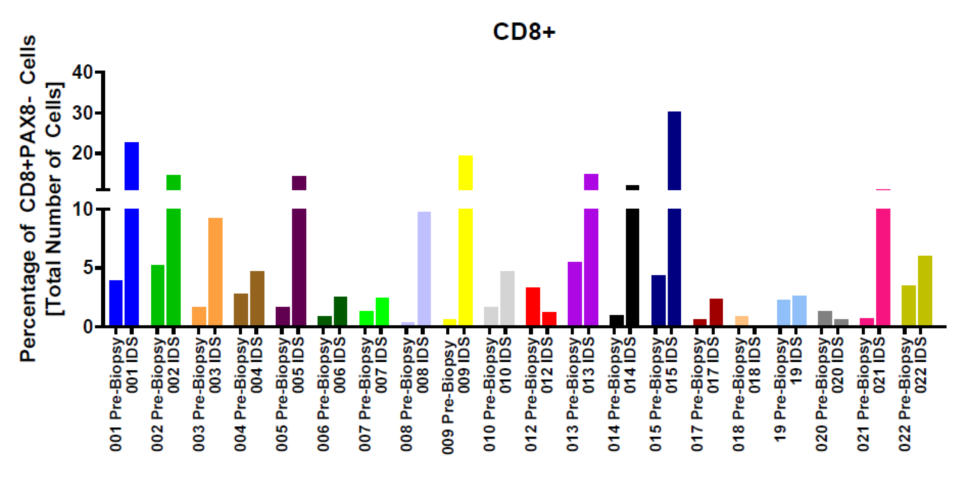
结论:在EOC高危人群中,前期化疗加用纳武单抗有利于PFS获益和肿瘤微环境的改善。
3、【126 - Featured Poster Session】Development of a predictive signatures for immune therapy in ovarian cancer: Whom to treat and whom not to treat?
卵巢癌免疫治疗预测性标志物的研究进展
目的:为了探究卵巢癌(OC)肿瘤微环境的免疫状况,挖掘预测性生物标记物来筛选免疫治疗的目标患者,我们发起了一项研究,综合分析在初始减瘤术、间歇性减瘤术和复发时采集的肿瘤样本的独特的分子学和组织病理学特征。方法:我们招募了60多名女性,并在30名女性中完成了单细胞RNA测序(ScRNAseq)、多重免疫组化分析、肿瘤浸润淋巴细胞(TILs)的H&E评分和NanoString分子亚型分析。研究中使用10X基因组学平台进行单细胞RNA测序。对共刺激因子基因表达模式、程序性细胞死亡蛋白及其配体PD-1和PDL-1进行分析。TIL评分采用Salgado标准,PDL-1/PD-1 IHC染色采用肿瘤比例评分(TPS)和联合比例评分(CPS)进行评估。结果:ScRNAseq发现所有类型细胞(1%-22%)都进行分析时,23/30(76%)患者可检测到PD-1及PDL-1基因表达,而只对免疫细胞及上皮细胞进行分析时,20/30(66%)患者可检测到PD-1及PDL-1基因表达,这两种基因在4/30(12%)患者中的表达率最高。ScRNAseq检测的PDL-1基因水平在IHC检测的高表达和低表达范围内表现出一致的线性关系。ScRNAseq具备其他基因检测所没有的优势,即能够在没有PDL-1免疫组化染色的肿瘤样本上检测到PDL-1基因。PD-1/PDL-1基因在4种分子亚型中的差异表达在免疫反应组中最高,有趣的是,这组中有2名患者没有检测到PD-1/PDL-1的表达,这表明单独的分子亚型可能无法预测免疫治疗的反应。4/30例(13%)和10/30例(33%)患者的间质TILs分别为50%~90%和20%~40%,但TIL评分与PD-1/PDL-1基因表达水平无相关性。结论:ScRNAseq在跨细胞鉴定PD-1/PD-L1方面比IHC法更可靠,单一生物标记物可能不能预测治疗反应。我们的研究还在继续,后期将根据是否有多种免疫标志物(PD-1/PDL-1,TIL,分子亚型,IHC检测)将这些患者分为不同的亚型,并随访其病程,这有助于识别出未来最有可能从免疫治疗中获益的患者,并进一步了解OC的免疫逃避机制。
4、【28 - Scientific Plenary】Tolerability and adverse events experienced by women with ovarian cancer treated with intravenous or intraperitoneal chemotherapy plus veliparib and bevacizumab based on BRCA status
基于BRCA状态的卵巢癌患者静脉或腹腔化疗联合veiliparib和贝伐珠单抗的耐受性和不良反应分析
目的:本研究旨在评估GOG I期临床研究(GOG 9923,NCT00989651)中,不同BRCA状态患者对静脉或腹腔化疗联合veiliparib和贝伐珠单抗治疗的耐受度。方法:本研究是一项机构审查委员会批准的多机构前瞻性研究,研究对象接受卡铂、紫杉醇和贝伐珠单抗(Q3w,方案1),或卡铂,周疗紫杉醇和贝伐珠单抗(方案2),或紫杉醇、贝伐珠单抗联合顺铂腹腔化疗(方案3)。所有治疗方案后贝伐珠单抗均作为维持治疗持续使用。在每个治疗周期内每天(连续方案)或在周期第2-5天(间歇方案)给予每日两次Veliparib作为细胞毒性治疗。最大耐受剂量(MTD)和推荐的II期临床剂量作为主要终点,在2019年ASCO大会中报道。本文是基于BRCA状态的计划外的事后的临床特征和毒性数据分析,采用描述性统计和Kaplan-Meier方法。结果:共评估了424例患者,其中173例(40.8%)采用方案1治疗,128例(30.2%)采用方案2治疗,123例(29%)采用方案3治疗。多数患者是50-69岁的白种人,ECOG评分0-1分。最常见的是浆液性癌(77.6%),其次为子宫内膜样癌(7.5%)和透明细胞癌(5.9%)。方案1中85%的患者出现4-5级毒性反应;方案2中比例为50%;方案3中比例为45.5%。方案1、方案2和方案3治疗的患者中分别有10%、12%和19.8%的BRCA突变阳性。与野生型患者相比,BRCA突变阳性患者的贫血(29.3% vs 27.2%,P=0.73)、粒缺伴发热(8.8% vs 9.1%,P=0.92)、腹痛(8.6% vs 4.8%,P=0.26)、结肠穿孔(1.7% vs 1%,P=0.62)、恶心(6.9% vs 6.2%,P=0.85)、呕吐(5.2% vs 4.8%,P=0.89)以及外周感觉神经病变(0% vs 1.4%,P=0.36)的发生率相似。尽管本研究的主要目标不是评估治疗结局,BRCA突变阳性和阴性患者的中位无进展生存期无显著差异(HR=0.96,95% CI 0.65-1.42)。结论:胚系BRCA基因突变对上皮性卵巢癌的化疗敏感性有显著影响,但也可能影响卵巢癌患者的药物毒性反应。然而,我们发现在新诊断卵巢癌人群中,不论BRCA基因突变与否,患者都能耐受治疗。
5、【26 Scientific Plenary】Demcizumab combined with paclitaxel for platinum-resistant ovarian, primary peritoneal, and fallopian tube cancer (EOC): The SIERRA multi-institutional open-label phase Ib trial.
Demcizumab联合紫杉醇治疗铂耐药卵巢癌、原发性腹膜癌和输卵管癌(EOC): SIERRA多机构开放标签Ib期研究
目的:我们的目标是对demcizumab (DLL4靶向IgG2人源化单克隆抗体;Notch通路的有效抑制剂)与紫杉醇周疗联合应用于铂耐药EOC的最大耐受剂量(MTD)或最大给药剂量(MAD)进行评估;以确定第二阶段剂量。客观缓解率(ORR)是次要目标。方法:我们对铂耐药复发的EOC患者进行了3+3剂量爬坡试验,纳入患者为RECIST v. 1.1评估有可测量病灶,要求既往接受少于4线化疗方案。最初目标剂量组为2.5 mg/kg和5 mg/kg,如果5 mg/kg的剂量不能耐受,则用一个中等剂量3.5 mg/kg。Demcizumab于第1天和第15天静脉输入,紫杉醇(80 mg/m2 IV)在第1天、第8天和第15天使用,使用3个28天周期,如果安全的话,3个周期可以重复一次。此后,单独予紫杉醇,直到出现不可接受的毒性或疾病进展。结果:共入组19例(每剂量3例),未观察到剂量限制毒性(DLT);然而,根据demcizumab其他研究的安全数据,中剂量水平(3.5 mg/kg)被纳入(n=3)并扩大(n=10)。所有级别中最常见的不良事件是腹泻(68%)、疲劳(58%)、周围水肿(53%)和恶心(53%)。≥3级不良事件包括高血压(26%)、腹痛、贫血、中性粒细胞减少和尿毒症(各11%)。任何级别的demcizumab相关不良事件包括疲劳(42%)、高血压(37%)、腹泻(32%)和头痛(32%)。观察到2级(n=2)和1级(n=1)肺动脉高压。未记录DLTs,未达到MTD。ORR为21% (95% CI 6-45%);临床有效率(CBR)为42% (95% CI 20-66%)。5例既往接受贝伐珠单抗治疗的患者中,2例为客观缓解,2例为病情稳定(≥12周)。图1
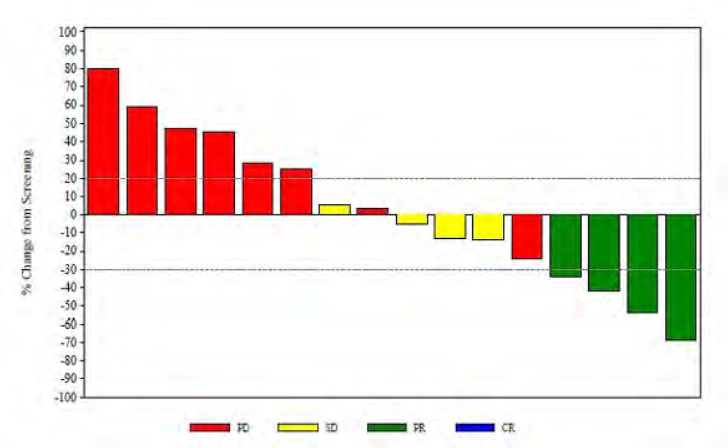
图1:瀑布图最大百分比减低反映了肿瘤体积减少的最佳整体缓解。PD:疾病进展;SD疾病稳定;PR:部分缓解;CR:完全缓解。结论:Demcizumab联合紫杉醇毒性可控,并且在重度铂耐药性卵巢癌患者中表现出抗肿瘤活性。下一代双特异性VEGF/DLL4抗体、navicixizumab联合紫杉醇的相关研究正在进行中。
6、【81 - Scientific Plenary】Patient preferences for side effects and decision-making factors associated with maintenance therapy for ovarian cancer
患者对与卵巢癌维持治疗相关的副作用和决策因素的倾向性
目的:卵巢癌患者现在有不同的维持治疗的选择。考虑到接受维持治疗的时间延长,我们评估了患者对潜在副作用和决策因素的倾向性。方法:作为一项关于维持治疗的共同决策的大型研究的一部分,我们在面对面的结构化访谈中使用问诊模拟评分(VAS)来评估晚期卵巢癌患者的治疗倾向性。患者被要求对与化疗和维持治疗相关的副作用进行评价(0=最讨厌,100=最不讨厌)。患者也被要求评估与考虑维持治疗相关的决策因素(0=最不重要,100=最重要)。根据临床和人口特征因素评估VAS评分的差异。结果:共34例中位年龄64岁(37-76岁)的患者完成了访谈;53%的患者患有复发性卵巢癌;71%的人具有大学学历;62%的患者接受了维持治疗;77%的患者已婚/有伴侣。表1列出了总体VAS评分的中位数。既往接受贝伐珠单抗治疗的患者比未接受贝伐珠单抗治疗的患者更少受到高血压和贫血的困扰(分别为VAS=65 vs 30, P=0.03;52vs 14,P=0.001)。既往接受过PARPi治疗的患者比未接受过PARPi治疗的患者较少受到肺炎的困扰(分别为70 vs 36,P=0.03)。具有大学及以上学历的患者比学历较低的患者更少受到副作用的困扰,尤其是疲劳(32 vs 6,P=0.002)、皮疹(70 vs 18,P=0.02)和味觉变化(70 vs 30,P=0.02)。Table 1.Median overall VAS scores (N=34 pts).
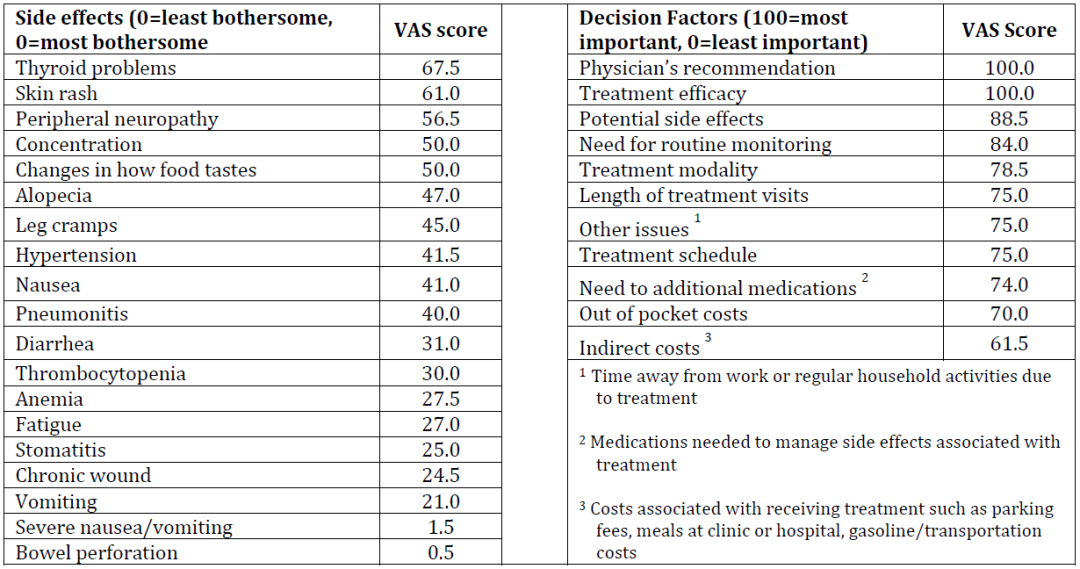
在决策因素方面,基于BEV或PARPi的治疗组之间差异不显著;然而,之前接受过维持治疗的患者认为额外的药物治疗的需求比从未接受过维持治疗的患者更重要(82vs 50,P=0.03)。相较于具有大学及以上学历的患者,受教育程度较低的患者认为所有决策因素更重要,特别是是否需要额外的药物(88 vs 60,P=0.009)、实际支付的费用(92 vs 59,P=0.03)、其他费用(83 vs 47,P=0.001)和治疗模式(85 vs 58,P=0.02)。相比已婚/有伴侣的患者,未婚/没有伴侣的患者认为治疗计划更重要(97比71,P=0.009)。家庭收入小于 版面编辑:洪山 责任编辑:卢宇
本内容仅供医学专业人士参考
相关搜索
卵巢癌
 京公网安备 11010502033352号 京卫计网审[2015] 第0203号
京公网安备 11010502033352号 京卫计网审[2015] 第0203号 京公网安备 11010502033352号 京卫计网审[2015] 第0203号
京公网安备 11010502033352号 京卫计网审[2015] 第0203号



